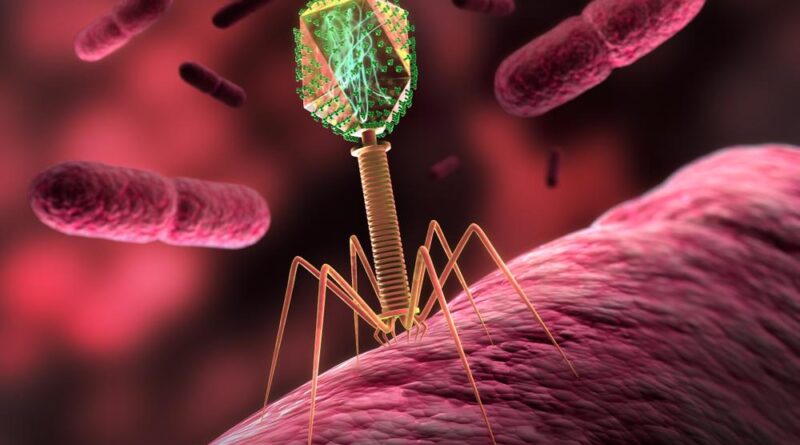
Jak bakteriofagi mogą zastąpić antybiotyki?
Jak bakteriofagi mogą zastąpić antybiotyki? Kompletny przewodnik po terapii fagowej
Rosnąca oporność na antybiotyki sprawia, że medycyna pilnie potrzebuje skutecznych alternatyw. Coraz częściej na pierwszym planie pojawiają się bakteriofagi – wirusy atakujące bakterie, które w wielu przypadkach mogą zastąpić lub uzupełnić antybiotyki. W tym artykule wyjaśniamy, jak działa terapia fagowa, kiedy ma sens, jakie są jej zalety i ograniczenia oraz jak wygląda dostęp do fagów w Polsce i na świecie.
Wprowadzenie: Dlaczego temat bakteriofagów jest dziś tak ważny?
Według Światowej Organizacji Zdrowia antybiotykooporność należy do najpoważniejszych zagrożeń dla zdrowia publicznego. Wzrost liczby zakażeń wywołanych przez bakterie wielolekooporne (MDR) – jak MRSA, Pseudomonas aeruginosa, Klebsiella pneumoniae czy Acinetobacter baumannii – powoduje, że standardowe leczenie bywa nieskuteczne. Bakteriofagi oferują precyzyjne, wirusowe „pociski”, które są w stanie celować w konkretne bakterie, nie naruszając przy tym całej mikrobioty.
Czym są bakteriofagi i jak działają?
Bakteriofagi (fagi) to naturalnie występujące wirusy, które infekują i niszczą bakterie. Wyróżnia je:
- Wysoka swoistość: każdy fag atakuje zwykle wąski zakres szczepów danej bakterii;
- Cykl lityczny: fag wstrzykuje do komórki bakteryjnej swój materiał genetyczny, namnaża się i doprowadza do lizy (rozpadu) bakterii;
- Samopowielanie w ognisku zakażenia: o ile bakterie docelowe są obecne, fag może się namnażać, wzmacniając efekt terapeutyczny;
- Naturalne pochodzenie: fagi są wszechobecne w środowisku, a kontakt człowieka z fagami jest codziennością.
W kontekście leczenia najczęściej stosuje się fagi lityczne, unikając fagów lizogennych (mogących wbudować się w genom bakterii), aby zminimalizować ryzyko przeniesienia genów oporności.
Dlaczego bakteriofagi mogą zastąpić antybiotyki?
Choć antybiotyki pozostają fundamentem leczenia infekcji, fagi coraz częściej są rozważane jako alternatywa lub uzupełnienie. Oto kluczowe powody:
- Skuteczność wobec bakterii opornych: gdy antybiotyki zawodzą, dopasowane fagi mogą niszczyć nawet wielolekooporne szczepy.
- Celowanie w biofilm: niektóre fagi produkują enzymy (np. depolimerazy), które rozbijają biofilm – tarczę ochronną bakterii na implantach i ranach przewlekłych.
- Phage-antibiotic synergy (PAS): połączenie fagów z antybiotykami bywa silniejsze niż każda z metod z osobna.
- Mniejsze zaburzenia mikrobioty: swoistość fagów ogranicza „zamiatanie” pożytecznych bakterii, co zmniejsza ryzyko dysbiozy.
- Elastyczność: możliwość tworzenia koktajli fagowych i szybkiego „przeprogramowania” panelu fagów pod konkretny szczep.
Antybiotyki vs bakteriofagi – szybkie porównanie
| Cecha | Antybiotyki | Bakteriofagi |
|---|---|---|
| Zakres działania | Szeroki | Bardzo wąski (wysoka swoistość) |
| Wpływ na mikrobiotę | Często znaczący | Minimalny |
| Ryzyko oporności | Wysokie i rosnące | Możliwe, ale można przełamać doborem nowych fagów |
| Biofilm | Trudny do penetracji | Enzymy fagowe mogą rozbijać biofilm |
| Produkcja | Standaryzowana | Personalizowana lub koktajle; wymagane testy dopasowania |
| Regulacje | Szeroko dopuszczone | Ramy prawne wciąż się rozwijają |
Zastosowania kliniczne i jakość dowodów
Najlepiej udokumentowane wskazania do terapii fagowej dotyczą przewlekłych, miejscowych i trudnych do leczenia zakażeń:
- Zakażenia ran przewlekłych i oparzeń (np. Pseudomonas aeruginosa, Staphylococcus aureus): udokumentowane przypadki poprawy, w tym przełamywanie biofilmu.
- Zakażenia protez i implantów (stawy, siatki, zastawki): fagi stosowane miejscowo i systemowo, nierzadko w połączeniu z chirurgią i antybiotykami.
- Infekcje układu oddechowego (np. u chorych na mukowiscydozę): obiecujące studia przypadków, zwłaszcza wobec P. aeruginosa.
- Zakażenia układu moczowego (MDR E. coli, Klebsiella): doniesienia o skuteczności terapii dostosowanej do szczepu.
- Zakażenia kości i szpiku (osteomyelitis): terapia łączona z chirurgią i antybiotykami.
Chociaż istnieją spektakularne studia przypadków (m.in. terapia spersonalizowana w rozległych zakażeniach Mycobacterium abscessus opornych na leczenie), duże, wieloośrodkowe randomizowane badania nadal są w toku lub nieliczne. Wczesne badania (np. w oparzeniach) pokazały zarówno potencjał, jak i wyzwania jakościowe (stabilność i dobór fagów). Najnowsze projekty kliniczne w Europie i USA rozwijają standardy produkcji i oceny skuteczności fagów, a rosnąca liczba rejestracji badań klinicznych zwiększa bazę dowodową.
Jak wygląda terapia fagowa w praktyce?
- Identyfikacja patogenu: pobiera się próbki z ogniska zakażenia i wykonuje szczegółową diagnostykę (w tym antybiogram).
- Fagogram: laboratorium testuje panel fagów przeciwko konkretnemu szczepowi, by sprawdzić wrażliwość bakterii.
- Dobór i przygotowanie koktajlu: komponuje się mieszankę 2-5 (lub więcej) fagów celujących w ten sam szczep, by ograniczyć ryzyko oporności.
- Wytwarzanie i kontrola jakości: filtry endotoksyn, badania czystości, standaryzacja dawki, najlepiej w warunkach zbliżonych do GMP.
- Droga podania: miejscowo (żele, irygacje), doustnie, inhalacyjnie (nebulizacja), dostawowo, a w specjalnych przypadkach – dożylnie.
- Monitorowanie: ocena kliniczna, powtarzane posiewy, ewentualny retest fagogramu; czas terapii może wynosić od kilku dni do kilku tygodni.
Gdzie terapia fagowa jest dostępna?
- Polska: terapia fagowa jest prowadzona w ramach procedur eksperymentalnych w wyspecjalizowanych ośrodkach (m.in. jednostki badawcze, programy w Instytucie we Wrocławiu). Wymaga kwalifikacji i współpracy lekarza.
- Gruzja (Tbilisi): ośrodek Eliava Institute ma najdłuższą tradycję fagoterapii.
- Belgia: funkcjonuje tzw. model „magistralny”, umożliwiający personalizowane preparaty fagowe na indywidualne zamówienie.
- USA i UE: możliwy dostęp w trybie „compassionate use”/„expanded access” oraz w ramach badań klinicznych; trwają prace nad standardami regulacyjnymi.
| Zakażenie | Typowe drogi podania | Status dowodów |
|---|---|---|
| Rany przewlekłe | Miejscowo, irygacje | Studia przypadków, małe badania |
| Infekcje implantów | Miejscowo + dożylne | Rosnąca liczba raportów |
| ZUM (MDR) | Doustnie, dopęcherzowo | Wczesne dane kliniczne |
| Infekcje oddechowe | Nebulizacja, doustnie | Studia przypadków |
Bezpieczeństwo, ryzyka i ograniczenia
- Bezpieczeństwo: dotychczasowe raporty wskazują na dobrą tolerancję; możliwe przejściowe reakcje (gorączka, miejscowe podrażnienie), rzadko reakcje immunologiczne.
- Endotoksyny: szybka liza dużej populacji bakterii Gram-ujemnych może uwalniać endotoksyny; dlatego ważna jest kontrola jakości i dobór drogi podania.
- Oporność bakterii na fagi: bakterie mogą nabywać oporność, ale można ją przełamać rotacją fagów lub koktajlami; łączenie z antybiotykami (PAS) dodatkowo ogranicza ryzyko.
- Swoistość: zaleta kliniczna, ale wymaga wykonania fagogramu i personalizacji.
- Standaryzacja i regulacje: wciąż rozwijane; nie wszystkie kraje mają jasne ścieżki rejestracyjne.
Czy bakteriofagi naprawdę mogą zastąpić antybiotyki?
Krótkie podsumowanie kluczowych scenariuszy:
- Gdy antybiotyki zawodzą: w infekcjach wywołanych przez bakterie wielolekooporne spersonalizowana terapia fagowa może stanowić realną alternatywę i doprowadzić do eradykacji patogenu.
- W biofilmie i zakażeniach przewlekłych: fagi mogą być skuteczniejsze od samego antybiotyku dzięki enzymom rozbijającym biofilm i zdolności penetracji struktur bakteryjnych.
- W strategii łączonej: często najlepsze efekty daje połączenie fagów z antybiotykiem, wykorzystujące zjawisko PAS i ograniczające rozwój oporności.
- W praktyce populacyjnej: na poziomie zdrowia publicznego fagi prawdopodobnie będą uzupełnieniem antybiotyków, a nie pełnym zamiennikiem – przynajmniej do czasu ugruntowania dowodów i regulacji.
Praktyczne wskazówki dla pacjentów i lekarzy
- Nie odstawiaj samodzielnie antybiotyków: decyzje o terapii podejmuj z lekarzem.
- Zadbaj o dokumentację: aktualne posiewy, antybiogramy i historia leczenia są kluczowe do kwalifikacji do fagoterapii.
- Zapytaj o fagogram: to test wrażliwości bakterii na konkretne fagi – warunek skuteczności terapii.
- Rozważ terapię łączoną: wiele ośrodków stosuje fagi wraz z antybiotykami i procedurami chirurgicznymi.
- Monitoruj efekty i działania niepożądane: regularne kontrole ułatwiają modyfikację terapii.
- Wybieraj doświadczone ośrodki: ważne są standardy jakości, czystości i właściwy dobór fagów.
Innowacje: od koktajli fagowych po fagi inżynieryjne
- Koktajle fagowe: mieszanki kilku fagów rozszerzają zakres działania i utrudniają powstanie oporności.
- Fagi modyfikowane genetycznie: np. z „wyciszonymi” genami lizogennymi lub wzbogacone o enzymy przeciw biofilmowi – obszar badań o dużym potencjale.
- Enzymy fagowe (endolizyny): białka pochodzenia fagowego, które same w sobie mogą zabijać bakterie – alternatywa dla całych wirionów.
- Diagnostyka fagowa: fagogramy i szybkie testy wrażliwości skracają czas doboru terapii.
FAQ: Najczęstsze pytania o bakteriofagi
Czy fagi działają na wirusy lub grzyby?
Nie. Bakteriofagi są specyficzne wyłącznie dla bakterii.
Ile trwa terapia fagowa?
Od kilku dni do kilku tygodni, zależnie od lokalizacji zakażenia, drogi podania i odpowiedzi klinicznej.
Czy pojawia się oporność na fagi?
Może, ale jest zwykle łatwiejsza do obejścia niż oporność na antybiotyki – stosuje się rotację lub koktajle fagowe oraz łączy fagi z antybiotykami.
Czy są dostępne gotowe, „uniwersalne” preparaty?
W medycynie człowieka dominuje personalizacja i koktajle dobrane do szczepu. Istnieją natomiast zarejestrowane preparaty fagowe dla bezpieczeństwa żywności.
Mini-poradnik: kiedy rozważyć bakteriofagi?
| Sytuacja kliniczna | Rozważenie fagów | Notatka |
|---|---|---|
| MDR zakażenie ran | Tak | Fagogram + terapia łączona |
| Biofilm na implancie | Tak | Wsparcie chirurgii |
| Łagodne ZUM wrażliwe na antybiotyk | Raczej nie | Najpierw standard |
| Mukowiscydoza z MDR P. aeruginosa | Tak | Badania i case studies |
| Sepsa | Ostrożnie | Eksperymentalnie, w ośrodkach |
SEO – kluczowe frazy, które warto znać
Jeśli szukasz informacji, pomocne będą takie hasła, jak: bakteriofagi, terapia fagowa, fagoterapia w Polsce, jak bakteriofagi mogą zastąpić antybiotyki, antybiotykooporność, biofilm, MRSA, Pseudomonas aeruginosa, Klebsiella pneumoniae, zakażenia przewlekłe, koktajl fagowy, fagogram, phage-antibiotic synergy.
Podsumowanie i wnioski
Czy bakteriofagi mogą zastąpić antybiotyki? W wielu trudnych przypadkach – tak, szczególnie gdy mamy do czynienia z bakteriami wielolekoopornymi i biofilmem. Z praktycznego punktu widzenia obecnie najlepiej traktować fagi jako silne uzupełnienie arsenału terapeutycznego, które w wyjątkowych sytuacjach może pełnić rolę alternatywy dla antybiotyków. Kluczem do sukcesu jest prawidłowa diagnostyka, fagogram, dobór koktajlu oraz – często – terapia skojarzona.
W najbliższych latach spodziewajmy się rozwoju regulacji, standaryzacji jakości i rosnącej liczby badań klinicznych. To szansa na bezpieczniejsze, spersonalizowane leczenie, które pozwoli skuteczniej odpowiadać na globalne wyzwanie, jakim jest oporność na antybiotyki.
Jeśli rozważasz terapię fagową, porozmawiaj z lekarzem lub skontaktuj się z wyspecjalizowanym ośrodkiem. Przygotuj dokumentację medyczną, wyniki posiewów i antybiogramy – to pierwszy krok do spersonalizowanego leczenia.